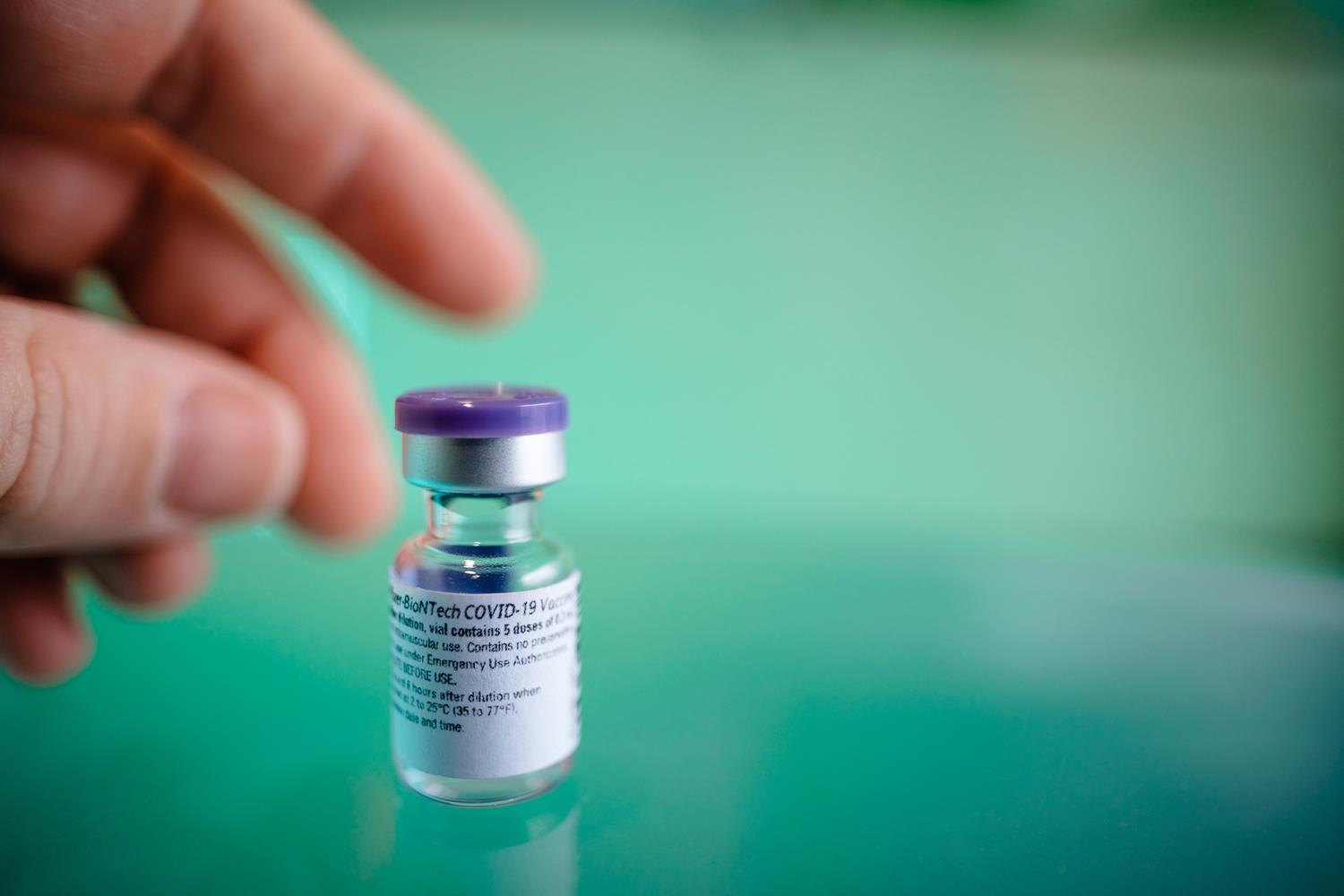
Kanada jako pierwszy kraj na świecie pozwoliła na stosowanie szczepionki firm Pfizer i BioNTech u osób od 12. do 15. roku życia.
Unia Europejska i Europejska Agencja Leków (EMA) prawdopodobnie zgodę wydadzą w połowie czerwca na użycie tej szczepionki w grupie wiekowej 12-15 lat.
W Stanach Zjednoczonych taka decyzja może już zapaść w tym tygodniu.
W badaniach tej firmy uczestniczyło 2260 nastolatków. U osób, które otrzymały preparat, żadna z nich nie zachorowała. Zatem szczepionka ta wykazała 100-procentową skuteczność przeciw COVID-19.
Izrael. Skuteczność szczepionki na COVID-19 firmy Pfizer
Z publikacji w „The Lancet” z danych z Izraela między 24 stycznia a 3 kwietnia 2021 roku wynika, że dwie dawki szczepionki na COVID-19 Pfizer zapewniają ponad 95 proc. ochrony przed zakażeniem, ostrym przebiegiem choroby i śmiercią.
Dokładniej – po upływie 14 dni od otrzymania drugiej dawki – szczepionka zapewnia 96,5 proc. ochrony przed zakażeniem, 98 proc. ochrony przed hospitalizacją i 98,1 proc. ochrony przed zgonem.
Jedna dawka szczepionki już zapewnia 58 proc. ochrony przed zakażeniem, 76 proc. ochrony przed hospitalizacją oraz 77 proc. ochrony przed zgonem.
Trzecia dawka szczepionki
Szef firmy BioNTech Ugur Sahin ogłosił, że potrzebny będzie podanie trzeciego zastrzyku, aby podnieść odporność do prawie 100 procent. Skuteczność tej szczepionki od jej podania po pół roku spada do 91 procent.
Trzeci zastrzyk ma być podany w okresie 9-12 miesięcy po pierwszej dawki szczepionki. Zaś kolejny zastrzyk co roku lub co 18 miesięcy.
Pfizer rozpoczął testy leku na COVID-19
Prawdopodobnie na rynek trafi jeszcze w tym roku.
Jest to terapia doustna, która będzie podawana przy pierwszych oznakach infekcji, bez konieczności hospitalizacji.
Pigułka ma zapobiegać działaniu wirusa w płucach, gardle i nosie.
Szczegółowe informacje o Pfizer / BioNTech
Pfizer i BioNTech rozpoczynają badanie w ramach szerszego planu rozwoju, którego celem jest poddanie ocenie dawki przypominającej szczepionki przeciw COVID-19 i jej nowych wariantów
Pfizer i BioNTech ogłosiły, że trwa proces oceny bezpieczeństwa i immunogenności trzeciej dawki szczepionki Pfizer-BioNTech przeciw COVID-19 (BNT162b2), aby przeanalizować wpływ dawki przypominającej na odporność przeciw chorobie COVID-19 wywołanej przez obecne i ewentualne nowe szczepy wirusa SARS-CoV-2. W badaniu wezmą udział uczestnicy badania fazy I w Stanach Zjednoczonych, którym zaoferuje się możliwość otrzymania dawki przypominającej 30 µg obecnej szczepionki w 6 do 12 miesięcy po podaniu pierwotnej szczepionki w schemacie dwudawkowym. Badanie wpisuje się w strategię firm dotyczącą rozwoju klinicznego szczepionki, a celem jest określenie skuteczności trzeciej dawki przeciwko ewoluującym wariantom wirusa.
Aby przygotować się na wszelkie ewentualne zmiany mogące zajść w szczepach wirusa w przyszłości, firmy Pfizer i BioNTech prowadzą rozmowy z agencjami rejestracyjnymi, w tym z Amerykańską Agencją Żywności i Leków (FDA) i Europejską Agencją Leków, dotyczące badania klinicznego umożliwiającego rejestrację szczepionki, którego przedmiotem będzie dokonanie oceny szczepionki specyficznej dla danego wariantu o zmodyfikowanej sekwencji mRNA. W badaniu wykorzystano by nową formułę szczepionki Pfizer-BioNTech, powstałą w oparciu o wariant B.1.351, których po raz pierwszy został zidentyfikowany w RPA. Umożliwiłoby to firmom szybkie dostosowanie obecnej szczepionki w celu zapewnienia ochrony przed COVID-19, którą wywołują obecne szczepy. Kierując się zaktualizowanymi wytycznymi wydanymi przez FDA dotyczącymi stosowania szczepionek w sytuacji wyjątkowej w celu zapobiegania chorobie COVID-19, zawierającymi zalecenia dotyczące oceny skuteczności zmodyfikowanej szczepionki wobec wariantów wirusa, firmy mają nadzieję kontynuować proces weryfikacji zmodyfikowanych szczepionek mRNA, w przypadku których proces rejestracyjny będzie zbliżony do rozwiązań znanych ze szczepionek przeciw grypie.
„Chociaż brak dowodów na to, że obecne warianty wirusa powodują utratę ochrony zapewnianej przez naszą szczepionkę, podejmujemy wiele zdecydowanych działań, aby odpowiednio przygotować się na to, że szczepionka nie będzie wykazywać skuteczności wobec nowego szczepu. Badanie dotyczące dawki przypominającej jest ważne, ponieważ pozwoli poddać analizie bezpieczeństwo trzeciej dawki i uzyskiwaną odporność na obecne szczepy” – powiedział Albert Bourla, prezes i dyrektor generalny firmy Pfizer. „Dokonujemy odpowiednich inwestycji i prowadzimy rozmowy z agencjami rejestracyjnymi, aby przygotować się do opracowania i uzyskania dopuszczenia do stosowania – w razie potrzeby – zaktualizowanej wersji szczepionki mRNA lub dawki przypominającej”.
„Nasza strategia proaktywnego rozwoju klinicznego szczepionki ma na celu stworzenie odpowiednich warunków już dziś, które pozwolą nam sprostać wyzwaniom jutra. Chcemy być przygotowani na różne scenariusze ” – powiedział Ugur Sahin, prezes i współzałożyciel BioNTech. „Będziemy poddawać ocenie drugą dawkę przypominającą w obecnym schemacie, jak również przygotujemy się do ewentualnego szybkiego dostosowania szczepionki do nowych wariantów wirusa, które mogą okazać się odporne na obecną wersję naszej szczepionki na bazie mRNA. Dzięki elastyczności naszej zastrzeżonej platformy szczepionek wykorzystujących technologię mRNA, jesteśmy przygotowani pod względem technicznym do opracowania szczepionek przypominających w ciągu kilku tygodni, jeśli zajdzie taka potrzeba. Takie podejście stosuje się już w przypadku innych chorób zakaźnych, takich jak grypa. Podejmujemy te działania, aby zapewnić długotrwałą odporność na wirusa i jego odmiany”.
Podanie trzeciej dawki BNT162b2 pozwoli wstępnie ocenić jej bezpieczeństwo i immunogenność. W badaniu weźmie udział 144 uczestników badania fazy I w dwóch kohortach wiekowych – 18–55 i 65–85 lat. Aby poddać ocenie możliwość zwiększenia skuteczności BNT162b2, badanie obejmie tych uczestników, którzy otrzymali dwie dawki szczepionki w badaniu fazy I od 6 do 12 miesięcy temu. Dzięki temu badaniu poddane zostanie bezpieczeństwo i tolerancja trzeciej dawki szczepionki, niezależnie od miana przeciwciał u uczestników badania. Uczestnicy zostaną przebadani przy podawaniu trzeciej dawki, a następnie tydzień i miesiąc później. Pfizer i BioNTech planują zbadać skuteczność neutralizacji omawianych szczepów wirusa SARS-CoV-2 przez surowice tych uczestników. Uczestnicy będą monitorowani w ramach badania przez maksymalnie 2 lata, zgodnie z pierwotnym planem.
Pfizer rozpoczyna badanie fazy I nowego doustnego przeciwwirusowego środka terapeutycznego przeciw SARS-CoV-2
Przeprowadzone dotychczas badania in vitro wskazują na to, że cząsteczka PF-07321332 jest mocnym inhibitorem proteazy o silnym działaniu przeciw wirusowi SARS-CoV-2
Jest to pierwszy podawany doustnie badany inhibitor proteazy specyficznej dla koronawirusa, który przechodzi do fazy badań klinicznych. Wcześnie rozpoczęły się badania kliniczne nad inhibitorem proteazy firmy Pfizer podawanej dożylnie. Na ten moment dożylny inhibitor proteazy, oceniany jest w badaniu fazy Ib z zastosowaniem wielu dawek preparatu w grupie hospitalizowanych uczestników badania klinicznego chorych na COVID-19.
Firma Pfizer ogłosiła w marcu, że przechodzi do badań metodą wielorazowej dawki rosnącej po zakończeniu badań metodą jednorazowej dawki rosnącej innowacyjnego przeciwwirusowego leku doustnego przeciw SARS-CoV-2. Badanie fazy I przeprowadzono u zdrowych osób dorosłych w celu oceny bezpieczeństwa i tolerancji eksperymentalnego, innowacyjnego przeciwwirusowego leku doustnego przeciw SARS-CoV-2, wywołującego chorobę COVID-19. Badanie fazy I jest prowadzone w Stanach Zjednoczonych. Podawany doustnie potencjalny lek przeciwwirusowy PF-07321332, inhibitor proteazy 3CL wirusa SARS-CoV-2, wykazał silną aktywność in vitro przeciw wirusowi SARS-CoV-2, a także aktywność przeciw innym koronawirusom, co sugeruje możliwość jego zastosowania w leczeniu COVID-19 oraz w zwalczaniu przyszłych zagrożeń związanych z koronawirusami.
„Walka z pandemią COVID-19 wymaga zarówno profilaktyki poprzez szczepienia, jak i ukierunkowanego leczenia osób zarażonych wirusem. Biorąc pod uwagę mutowanie wirusa SARS-CoV-2, oraz wszechstronnie negatywny wpływ COVID-19, dostęp do terapii zarówno teraz, jak i po pandemii będzie miał kluczowe znaczenie” – powiedział dr n. med. Mikael Dolsten, dyrektor naukowy i prezes Worldwide Research, Development and Medical w Pfizer.
„Zamysłem przy projektowaniu PF-07321332 było stworzenie potencjalnego doustnego produktu leczniczego, który może być przepisywany pacjentom nie wymagającym hospitalizacji i nie będących w stanie krytycznym już przy pierwszych oznakach infekcji. Jednocześnie potencjalny dożylny przeciwwirusowy produkt leczniczy firmy Pfizer to innowacyjna metoda leczenia pacjentów hospitalizowanych. Razem oba potencjalne produkty lecznicze, mogą stanowić całościowy paradygmat leczenia, stanowiący uzupełnienie do szczepień w przypadkach, gdy choroba będzie nadal występować”.
Inhibitory proteazy wiążą się z enzymem wirusowym (zwanym proteazą), zapobiegając replikacji wirusa w komórce. Inhibitory proteazy są skuteczne w leczeniu innych patogenów wirusowych, takich jak HIV i wirus zapalenia wątroby typu C, zarówno samodzielnie, jak i w połączeniu z innymi środkami przeciwwirusowymi. Dostępne obecnie na rynku produkty lecznicze działające na proteazy wirusowe zasadniczo nie wykazują toksyczności, dzięki czemu ta klasa cząsteczek może potencjalnie stanowić dobrze tolerowaną terapię przeciw COVID-19.
Badanie fazy I jest badaniem randomizowanym, podwójnie zaślepionym (ale otwartym dla sponsora), kontrolowanym placebo z zastosowaniem pojedynczej i wielokrotnej liczby dawek u zdrowych osób dorosłych, oceniającym bezpieczeństwo, tolerancję i farmakokinetykę PF-07321332.
Rozpoczęcie badania poprzedzono analizami przedklinicznymi, które wykazały aktywność przeciwwirusową tego potencjalnego, przełomowego produktu leczniczego przeciw SARS-CoV-2, zaprojektowanego specjalnie do powstrzymywania replikacji wirusa SARS-CoV-2. Struktura PF-07321332 wraz z danymi przedklinicznymi zostanie udostępniona 6 kwietnia podczas sesji poświęconej COVID-19 w ramach spotkania Spring American Chemical Society.
Pfizer kontynuuje także badania nad PF-07304814, podawanym dożylnie inhibitorem proteazy, w ramach badania wielodawkowego fazy Ib w grupie hospitalizowanych uczestników badania klinicznego, chorych na COVID-19.
Pfizer i BioNTech wnioskują do agencji regulacyjnych o rozszerzenie stosowania szczepionki przeciw COVID-19 w sytuacji wyjątkowej u młodzieży
9 kwietnia 2021 roku Pfizer Inc. (NYSE: PFE) i BioNTech SE (Nasdaq: BNTX) złożyły dziś wniosek o rozszerzenie zezwolenia na stosowanie w sytuacji wyjątkowej szczepionki Pfizer-BioNTech (BNT162b2) u młodzieży w wieku od 12 do 15 lat. W najbliższych dniach firmy planują złożyć wnioski do innych agencji regulacyjnych na całym świecie. Wnioski oparto na danych z kluczowego badania fazy III z udziałem młodzieży w wieku od 12 do 15 lat, do którego włączano osoby które w przeszłości przebyły lub nie przebyły zakażenia wirusem SARS-CoV-2, w którym wykazano 100% skuteczności i silną odpowiedź przeciwciał po podaniu szczepionki przeciw COVID-19.
Niedawno ogłoszono najważniejsze wyniki analizy skuteczności w ramach badania fazy III przeprowadzonego w gronie uczestników w wieku od 12 do 15 lat, w której uwzględniono przypadki COVID-19 odnotowane do 31 marca 2021 roku. Według wyników analizy szczepionka BNT162b2 była dobrze tolerowana, a działania niepożądane zasadniczo pokrywały się z tymi obserwowanymi u uczestników w wieku od 16 do 25 lat. Wszyscy uczestnicy badania będą monitorowani przez okres kolejnych dwóch lata po podaniu drugiej dawki, aby możliwa była ocena stopnia ochrony i bezpieczeństwa w długim okresie obserwacji.
Złożenie wniosków to ważny krok w działaniach prowadzonych przez Pfizer i BioNTech, które wspierają rządy w realizacji światowych programów szczepień. Firmy liczą na bliską współpracę z amerykańską Agencją Żywności i Leków (FDA) i innymi światowymi agencjami regulacyjnymi w działaniach ukierunkowanych na jak najszybsze rozszerzenie warunkowego pozwolenia lub dopuszczenia do stosowania w sytuacji wyjątkowej szczepionki przeciw COVID-19 u młodzieży w wieku od 12 do 15 lat.
Szczepionka Pfizer-BioNTech przeciw COVID-19, oparta na zastrzeżonej technologii mRNA firmy BioNTech, została opracowana zarówno przez BioNTech, jak i Pfizer. BioNTech jest podmiotem odpowiedzialnym w Unii Europejskiej oraz posiada dopuszczenie do stosowania w sytuacji wyjątkowej lub równoważną zgodę w Stanach Zjednoczonych (wspólnie z Pfizer), Wielkiej Brytanii, Kanadzie i innych krajach, poprzedzające złożenie wniosku o pozwolenie na dopuszczenie do obrotu na tych rynkach.